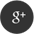Esta publicação também está disponível em:


A Síndrome de Eisenmenger (SE) permanece uma entidade clínica complexa e desafiadora que cursa com hipoxemia crônica e envolvimento multissistêmico incluindo eritrocitose secundária geralmente associada a deficiência de ferro, risco aumentado de fenômenos trombóticos e hemorrágicos assim como de arritmias, comprometimento renal, insuficiência cardíaca progressiva e morte prematura o que faz com que estes pacientes sejam melhor atendidos e conduzidos em centros de referência e sob uma visão multidisciplinar.
A síndrome descrita por Eisenmenger em 1897 foi definida, do ponto de vista fisiopatológico, em 1958 pelo Dr Paul Wood como “uma hipertensão pulmonar em níveis sistêmicos decorrente de uma alta resistência vascular pulmonar com consequente shunt bidirecional ou reverso ao nível atrial, ventricular ou aorto pulmonar”.
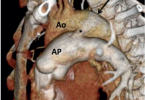
Esta grave entidade clínica é decorrente de amplos e não corrigidos defeitos intra ou extra cardíacos como defeitos do septo atrial, ventricular, shunts arteriais ou cardiopatias complexas sem restrição ao fluxo pulmonar.
Vamos abordar ao longo de 2 posts os principais aspectos envolvidos na Síndrome de Eisenmenger.
- Hipóxia crônica
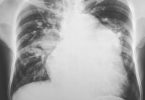
Usualmente se manifesta como cianose crônica, variando de leve a importante e piorando, tipicamente, com esforços. Pode não ser evidente em pacientes de pele escura ou naqueles com baixos níveis de hemoglobina.
Os seguintes achados estão relacionados com a hipóxia crônica apresentada por estes pacientes:
- Baqueteamento digital
- Disfunção renal
- Deficiência de ferro
- Eritrocitose secundária
Dica: sempre que colocarem baqueteamento digital em alguma questão de prova, lembre-se de cardiopatias congênitas que cursam com hipoxemia crônica. Não é a única causa, contudo. Dentro da própria cardiologia, temos que lembrar de outras causas como, por exemplo, a endocardite infecciosa subaguda.
- Eritrocitose
Como consequência da hipóxia crônica, observa-se um aumento na concentração de hemoglobina, aumento da massa eritrocitária e do hematócrito (eritrocitose secundária). Esta resposta corresponde a um mecanismo compensatório que aumenta a capacidade de transporte e distribuição de oxigênio para os tecidos periféricos. Está frequentemente associada a plaquetopenia que pode variar de leve a importante.
Uma fórmula proposta por Broberg e colaboradores tem sido utilizada para se calcular o nível de hemoglobina ideal para o paciente hipoxemiado:
Hemoglobina esperada= 57,5 – (0,44 X Sat O2)
A hipóxia crônica também tem sido associada a baqueteamento digital além de outros efeitos sistêmicos: disfunção renal, gota, cálculo biliar e osteoartropatia.
Hipóxia leva a uma disfunção renal decorrente da eritrocitose secundária e da hiperviscosidade, associada com glomerulopatia e doença renal tubular e intersticial. Em pacientes que se apresentam com disfunção renal de grau moderado a importante, drogas como diuréticos e anticoagulantes devem ser ajustadas. Nestes pacientes, terapia com drogas específicas para hipertensão arterial pulmonar devem ser consideradas.
Deficiência de ferro é um achado comum, ocorrendo em aproximadamente 1|3 dos pacientes e está associada com pior prognóstico. Esta alta prevalência de deficiência de ferro tem múltiplos fatores como: elevado requerimento, reduzida absorção intestinal, perda através do trato gastrointestinal ou outra via de sangramento. Suplementação de ferro oral pode ser dificultada pelos efeitos colaterais gastrointestinais associada com má absorção, além da resposta a longo prazo desta via de administração. Nestes casos deve ser considerada a via intravenosa para administração de ferro. Monitorização dos níveis de ferro devem ser acompanhados através dos níveis de ferritina e do índice de saturação da transferrina após uso de ferro intravenoso. Duração da suplementação oral deve ser individualizada.
Sangria de rotina não deve ser realizada em pacientes com Síndrome de Eisenmenger pelo risco de causar ou exacerbar deficiência de ferro e reduzir transporte de oxigênio tecidual aumentando o risco de acidente cerebrovascular.
Atencão: só considerar sangria para pacientes com níveis significativamente elevados de hemoglobina (acima de 22g/dL) ou hematócrito (65%) e que se apresentem com sintomas importantes de hiperviscosidade, na ausência de causas reversíveis como desidratação.
Este tipo de procedimento só deve ser realizado após discussão com profissional experiente. Deve ser retirado pequeno volume( 250 – 500ml ) com reposição simultânea para evitar desequilíbrio hemodinâmico.
- Sangramento e trombose
Estes pacientes apresentam risco elevado de sangramento e fenômenos trombóticos. Várias alterações são detectadas:
- alterações nas plaquetas
- anormalidades na cascata de coagulação
- alteração na função do fibrinogênio
- fatores de coagulação dependentes da vitamina K e fator V estão reduzidos
- atividade fibrinolítica está aumentada
- redução de multímeros do fator von Willebrand
Embora sangramentos (dentário, epistaxe, menorragia) possam ser de pequena monta e autolimitados, impactam na qualidade de vida do paciente. Hemoptise recorrente (secundária a hemorragia intrapulmonar e erosão de artérias bronquicas dilatadas) é a mais comum manifestação de sangramento com risco de vida potencial para o paciente. É uma causa incomum de morte e corresponde a cerca de 3% dos eventos fatais.
Eventos tromboembólicos (arterial e venoso) têm maior impacto na mortalidade dos pacientes com Síndrome de Eisenmenger. Trombose está associada com estase de sangue em cavidades cardíacas e artérias pulmonares dilatadas, arteriosclerose e\ ou disfunção endotelial, arritmias atriais e presença de material trombogênico (próteses ou enxerto). Trombo laminado pode estar presente em artérias pulmonares aneurismáticas, parcialmente calcificadas e ordem ser encontrados em mais de 30% dos pacientes. Infarto cerebrovascular pode ser causado por evento tromboembólico.
- Anticoagulação
Uso de anticoagulantes permanece controverso para estes pacientes, não sendo recomendado rotineiramente e devendo ser reservado para casos selecionados.
- Hemoptise
Deve ser instituído, de imediato, tratamento de infecção concomitante do trato respiratório. Fazer supressão de tosse. Reduzir atividade física. Correção de hipovolemia e anemia.
- Estratificação de risco
Evolução a longo prazo permanece desfavorável, com sobreviva em 5 anos estimada entre 74% e 81%.
Alguns fatores prognósticos isolados são descritos baseados em estudos retrospectivos; presença de síndrome de Down e shunt pré-tricuspídeo, idade mais avançada, progressão da hipóxia, classe funcional III ou IV ( NYHA ), redução da capacidade de exercício, biomarcadores séricos alterados ( pro BNP, PCR ), deficiência de ferro definido como uma saturação da transferrina abaixo de 20% e parâmetros ecocardiográficos de disfunção do VD
Semelhante a outras formas de HAP, piora clínica e história de hospitalização por IC são ambos relacionados com mortalidade.
No próximo post falaremos sobre como tratar pacientes com Síndrome de Eisenmenger.