Esta publicação também está disponível em:


Nos últimos anos, temos visto avanços significativos na área da medicina de precisão, especialmente no que diz respeito ao seu papel nas doenças cardiovasculares de origem mendeliana. Além do conhecimento habitual a respeito das clássicas Cardiomiopatia Hipertrófica (CMH) e Cardiomiopatia Não-Compactada, atualmente chamada de Ventrículo Esquerdo Não Compactado (VENC), temos uma forma de apresentação mista.
Relembrando os fenótipos clássicos:
Cardiomiopatia Hipertrófica:
A Cardiomiopatia Hipertrófica é a doença cardíaca genética mais comum, afetando cerca de 1:500 da população. Ela é transmitida de forma autossômica dominante e é causada por mutações em genes que codificam proteínas do sarcômero cardíaco. É caracterizada pela hipertrofia do músculo cardíaco, desarranjo das fibras miocárdicas e fibrose na ausência de outra causa identificável (HAS, doença valvar, coração de atleta). A doença pode se manifestar de diferentes formas, apresentando variações na anatomia do coração. O diagnóstico da CMH pode ser feito por meio de exames como o ecocardiograma e/ou ressonância cardíaca.
Principais genes associados:
| Gene | Frequência | Classificação ClinGen | |
| MYH7 | myosin heavy chain 7 | 15-25% | Definitivo |
| MYBPC3 | myosin binding protein C3 | 40-45% | Definitivo |
| TNNI3 | troponin I3 | 1-7% | Definitivo |
| TPM1 | tropomyosin 1 | 1-2% | Definitivo |
| MYL2 | myosin light chain 2 | 1-2% | Definitivo |
| MYL3 | myosin light chain 3 | 1-2% | Definitivo |
| ACTC1 | actin alpha cardiac muscle 1 | 1-2% | Definitivo |
| TNNT2 | troponin T2 | 1-7% | Definitivo |
| CSRP3 | cysteine and glycine rich protein 3 | <1% | Moderado |
| TNNC1 | troponin C1 | <1% | Moderado |
| JPH2 | junctophilin 2 | <1% | Moderado |
| ACTN2 | actinin alpha 2 | <1% | Moderado |
| PLN | phospholamban | <1% | Moderado |
| FHOD3 | formin homology 2 domain containing 3 | 0,5-2% | Não curado |
Ventrículo Esquerdo Não Compactado:
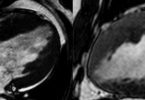
O Ventrículo Esquerdo Não Compactado é uma condição em que o músculo cardíaco apresenta trabéculas proeminentes e recessos inter-trabeculares profundos. Essa condição ocorre devido a falhas na compactação do miocárdio durante o desenvolvimento fetal, mas também como resultado de sobrecarga ventricular esquerda à outras patologias. Sua prevalência varia entre 0,014% e 1,3% dos pacientes que realizam ecocardiograma, em torno de 1:5000 da população. A condição pode ter origem esporádica ou hereditária, sendo a herança autossômica dominante mais comum. O diagnóstico geralmente é feito por meio de exames como o ecocardiograma transtorácico e/ou ressonância magnética cardíaca.
Principais genes associados:
| Gene | Frequência | Classificação Clingen | |
| MYH7 | myosin heavy chain 7 | 10-15% | Major gene |
| MYBPC3 | myosin binding protein C3 | 5-15% | Major gene |
| TTN | titin | 5-10% | Major gene |
| RYR2 | ryanodine receptor 2 | 1-2% | Rare |
| PRDM16 | PR/SET domain 16 | 1-2% | Rare |
| LBD3 | LIM domain binding 3 | 1-2% | Rare |
| ACTC1 | actin alpha cardiac muscle 1 | 1-5% | Rare |
| TBX5 | T-box transcription factor 5 | 1-2% | Rare |
| NKX2-5 | NK2 homeobox 5 | 1-2% | Rare |
| TAZ | Tafazzin | 1-2% | Rare |
| HCN4 | hyperpolarization activated cyclic nucleotide gated potassium channel 4 | 1-2% | Rare |
Recentemente, mutações em genes que codificam proteínas sarcoméricas, previamente implicadas na patogênese da cardiomiopatia hipertrófica, foram identificadas em pacientes com VE não compactado, mas sem hipertrofia de VE. Isso sugere que essas cardiomiopatias podem ter uma origem genética semelhante e, como alguns casos na literatura demonstram, a expressão fenotípica de ambas as doenças pode ocorrer no mesmo paciente.
Importância do Conhecimento Genético:
A medicina de precisão desempenha um papel fundamental na cardiologia, especialmente no diagnóstico e no tratamento de doenças cardíacas raras. Compreender as bases genéticas das condições cardíacas permite uma abordagem mais precisa e personalizada para cada paciente.
No caso da Cardiomiopatia Hipertrófica e do Ventrículo Esquerdo Não Compactado (VENC), identificar as mutações genéticas envolvidas é crucial para o diagnóstico precoce, o aconselhamento genético e a prevenção de complicações graves, como a morte súbita. Além disso, o conhecimento genético pode auxiliar na seleção de opções terapêuticas mais eficazes e na melhor compreensão da progressão da doença. Komissarova SM et al. (2020) descreveu probandos o fenótipo misto (CMH + VENC) em comparação com parentes de primeiro grau com CMH e VENC isolados, e os primeiros foram caracterizados por disfunção ventricular esquerda mais pronunciada (fração de ejeção, 43,57±7,6 e 53,64±6,51 %, respectivamente; p<0,001) e maior incidência de taquiarritmias ventriculares (7,9 e 2,2 %, respectivamente; p<0,01).
Em torno de 60 % das variantes nos genes MYH7 e MYBPC3, os quais codificam a cadeia pesada da β-miosina e a proteína C de ligação à miosina, respectivamente; são mais relacionados à expressividade de ambos fenótipos, bem como, denotam maior gravidade clínica e curso desfavorável. Lorca et al. (2015) estudaram três famílias com doenças VENC e CMH, com diferentes variantes em cada família e herança autossômica dominante; dentro de uma família, os investigadores descobriram a coexistência de ambas as doenças em dois pacientes, com possível candidato descrito: mutação da b-miosina cardíaca do sarcômero gene da cadeia pesada (MYH7 L620P). Nas outras duas famílias, a mesma variante foi descrita (MYBPC3 G263NX) com variabilidade fenotípica, e apenas um caso associando ambos VENC e CMH em cada família.
Mais estudos genéticos devem ser realizados a fim de buscar algumas respostas: CMH e VENC são doenças sobrepostas ou são manifestações distintas de um mesmo espectro de cardiomiopatia?
A compreensão das bases genéticas das doenças cardíacas permite um aconselhamento genético mais eficaz, ajudando os pacientes e suas famílias a entenderem a natureza hereditária dessas condições e a tomar medidas preventivas. À medida que a pesquisa genética avança, podemos esperar que novos genes relacionados às doenças cardíacas sejam descobertos, ampliando ainda mais nosso conhecimento e aprimorando o cuidado aos pacientes. A integração do conhecimento genético na prática clínica da cardiologia é essencial para proporcionar uma abordagem mais precisa e personalizada, melhorando a qualidade de vida e a sobrevida dos pacientes com doenças cardíacas genéticas.
Referências:
- Kelley-Hedgepeth A, Towbin JA, Maron MS. Images in cardiovascular medicine. Overlapping phenotypes: left ventricular noncompaction and hypertrophic cardiomyopathy. 2009 Jun 16;119(23):e588-9. doi: 10.1161/CIRCULATIONAHA.108.829564. PMID: 19528341.
- Boukhris M, Laaroussi L, Ben Salem N, Ben Halima A, Kachboura S. Left ventricular non-compaction and hypertrophic cardiomyopathy: two overlapping diseases or two manifestations of the same cardiomyopathy? Response to the letter concerning the article: “Left ventricular non-compaction associated with hypertrophic…. Kardiol Pol. 2017;75(7):727. doi: 10.5603/KP.2017.0133. PMID: 28703272.
- Komissarova SM, Rineiska NM, Chakova NN, Niyazova SS. [Overlapping Phenotype: Left Ventricular non-Compaction and Hypertrophic Cardiomyopathy]. Kardiologiia. 2020 Mar 18;60(4):137-145. Russian. doi: 10.18087/cardio.2020.4.n728. PMID: 32394868.
- Wilde AAM, et al. European Heart Rhythm Association (EHRA)/Heart Rhythm Society (HRS)/Asia Pacific Heart Rhythm Society (APHRS)/Latin American Heart Rhythm Society (LAHRS) Expert Consensus Statement on the State of Genetic Testing for Cardiac Diseases. Heart Rhythm. 2022 Jul;19(7):e1-e60. doi: 10.1016/j.hrthm.2022.03.1225. Epub 2022 Apr 4. PMID: 35390533.
- Lorca R, Martín M, Gómez J, et al. Hypertrophic cardiomyopathy and left ventricular non-compaction: Different manifestations of the same cardiomyopathy spectrum? Int J Cardiol. 2015; 190: 26–28, doi: 10.1016/j.ijcard.2015.04.138.