Esta publicação também está disponível em:


Os inibidores checkpoints do sistema imune (ICI) representam uma nova categoria de drogas que ajudam a direcionar o sistema imune para reconhecer as células alvo contra o câncer. Diversos ICI já foram aprovados no tratamento do câncer incluindo o melanoma, câncer de pulmão e carcinoma renal entre outros. Apesar de o bloqueio imune poder alcançar uma regressão importante do tumor, essa ativação sistêmica das células T pode levar a eventos adversos imunomediados como colite, pneumonites, miosites, dermatites, hipofisites, entre outros. (Para mais detalhes sobre cardiotoxicidade associada a tratamento para neoplasias, checar em https://d3gjbiomfzjjxw.cloudfront.net/cardiotoxicidade-dos-quimioterapicos-parte-01/ e também em https://d3gjbiomfzjjxw.cloudfront.net/cardiotoxicidade-dos-quimioterapicos-parte-02/)
Dentre os efeitos cardiovasculares dos ICI podemos citar: miocardites, doenças pericárdicas, vasculites, síndromes coronarianas agudas, eventos tromboembólicos e arritmias. O principal fator de risco para o evento cardiovascular é a combinação de diferentes ICI e o aparecimento dos eventos cardiovasculares geralmente é agudo, mas pode também acontecer depois de 6 meses do início do imunoterápico.
A fisiopatologia dos eventos cardiovasculares relacionados aos ICI é incerta. Entretanto, existem algumas hipóteses como: reação cruzada com células cardiovasculares; reação imunológica e diminuição da autotolerância levando ao reconhecimento de autoantígenos; ativação do sistema imunológico regulando autoanticorpos pré-existentes; liberação de citocinas pró-inflamatórias secundárias; desregulação do metabolismo miocárdico induzido pela inflamação.
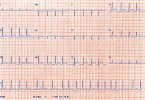
A miocardite é a manifestação cardiovascular mais comum com uma incidência entre 0,5 e 1.7%. Apesar da baixa incidência, o prognóstico da doença é muito ruim, com uma mortalidade que pode variar de 25 – 50% em curto prazo, por isso requer uma suspeição rápida e manejo precoce. A apresentação clínica geralmente começa com o aparecimento de algum sintoma cardiovascular associado a alterações eletrocardiográficas e mudanças em biomarcadores. Os principais achados clínicos e laboratoriais das alterações cardiovasculares relacionadas aos ICI estão descritos na tabela abaixo:
| Manifestação | Achados |
| Clínica | Dispneia, dor torácica, palpitações, choque, parada cardiorrespiratória |
| Eletrocardiograma | Pode ser normal (menos frequente), taquicardia, alargamento do QRS, prolongamento do QT, diminuição da voltagem do QRS, distúrbios de condução (bloqueios ou taquicardia ventricular) |
| Biomarcadores | Elevação de troponina (na miocardite pode estar elevada em 94% dos casos) |
| Ecocardiograma | Anormalidades das paredes ventriculares, redução da fração de ejeção do ventrículo esquerdo (na miocardite pode haver disfunção em menos 50% dos casos)
Alterações no strain global longitudinal (marcador prognóstico) |
| Ressonância Nuclear Magnética (RNM) | Alterações estruturais, edema miocárdico, realce tardio relacionado a miocardite |
| Biópsia Endomiocárdica (BEM) | Padrão ouro para miocardite. Infiltrado linfocítica com necrose miocárdica. |
O diagnóstico de miocardite proposto pela Sociedade Internacional de Cardio-Oncoclogia abrange:
– Diagnostico patológico – infiltrado inflamatório linfocítico na biópsia ou
– Diagnostico clínico – aumento de troponina + 1 critério maior ou 2 critérios menores (sempre excluindo outras causas cardiovasculares)
– Critérios maiores – RNM diagnóstica para miocardite (critérios de Lake Louise modificado)
– Critérios menores – sintomas clínicos, arritmias, queda da FEVE, outras efeitos imunomediados, RNM e BEM sugestivas, mas não diagnósticas.
Tratamento – a principal terapêutica para a miocardite relacionada aos ICI é pulso endovenoso de metilprednisolona seguidos de corticosteroides via oral com duração variável (até resolução de sintomas e queda de biomarcadores), podendo durar por pelo menos 6 – 12 semanas. Para casos refratários aos corticóides, o objetivo terapêutico é intensificar o tratamento imunossupressor com outras medicações: micofenolato mofetil, tacrolimus, abatacept, belatacept ou alentuzumabe. Pode se considerar também a plasmaférese para reduzir os níveis de citocinas circulantes.
Retorno da imunoterapia – o retorno dos ICI após uma complicação cardiovascular depende da severidade do quadro. Não é recomendado retornar com o tratamento oncológico depois de uma miocardite recuperada, mas essa conduta ainda não esta padronizada e deve ser individualizada.
Seguimento – não existe dado para definir um rastreamento de complicações cardiovasculares durante o uso dos ICI. Uma avaliação inicial com anamnese, ECG e troponina deveriam ser realizados. Durante a imunoterapia, os pacientes devem ser questionados sobre sintomas sugestivos.
Referências
Thuny F, Naidoo J, Neilan TG. Cardiovascular complications of immune checkpoint inhibitors for cancer. Eur Heart J. 2022 Aug 30:ehac456. doi: 10.1093/eurheartj/ehac456. Epub ahead of print. PMID: 36040835. https://academic.oup.com/eurheartj/advance-article-abstract/doi/10.1093/eurheartj/ehac456/6679177?redirectedFrom=fulltext&login=false