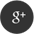Esta publicação também está disponível em:


Quando decidimos intervir em um paciente portador de valvopatia, a discussão sobre possibilidades terapêuticas acaba envolvendo possibilidades de implante de próteses e isso por si só seria um grande debate. Dentre essas possibilidades as próteses biológicas, ou biopróteses são alvo de muitas discussões e a deterioração de bioprótese é o centro dessa preocupação. Há pouco tempo formulou-se uma padronização de classificação com o intuito de alinhar nomenclaturas e também de padronizar questões prognósticas.
Inicialmente ocorre uma separação entre deterioração de bioprótese de natureza estrutural e não estrutural, sendo a localização específica da disfunção e o caráter de cronicidade determinantes para essa separação. Alterações que podem ser revertidas são sempre consideradas como não estrutrurais, mas a partir do ponto em que se cronificam, passam a ser estruturais.
Dentro das deteriorações estruturais, em casos de disfunção avançada e presença de sintomas, surge uma nova classificação de falência de bioprótese. De forma geral, uma vez que a deterioração progrida até a gerar repercussão hemodinâmica importante e há a necessidade de reintervenção ou mesmo o paciente tem um desfecho negativo por essa deterioração, você está diante de uma falência de bioprótese.
Evidentemente, além do tipo da prótese biológica e suas peculiaridades, a topografia em que ela é implantada pode fazer a diferença e quando observamos o volume de publicações, sem sombra de dúvidas a topografia aórtica é a que tem mais evidências no atual momento da cardiopatia estrutural.
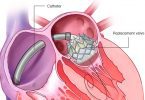
Por essa razão, há uma clara recomendação em realizar um exame de imagem no pós-intervenção imediato, seja de uma prótese convencional ou de uma prótese implantada por via percutânea. Conhecer o perfil hemodinâmico basal é fundamental para entendermos se no acompanhamento clínico algo está acontecendo.
O conceito de deterioração de bioprótese atualmente reside no surgimento de sintomas e nas elevações dos gradientes transprotéticos, acompanhados da redução da área protética efetiva, que muitos denominam área valvar. Algumas publicações recentes questionam qual o melhor método para realizar essa avaliação hemodinâmica e os questionamentos ficam entre a ecocardiografia, que é o padrão-ouro e a cateterização hemodinâmica, com medidas reais de gradientes. Diante da menor invasividade da ecocardiografia, esse método é o de escolha, mas entender suas limitações faz parte da interpretação adequada nesse tipo de avaliação.
É preciso entender os princípios da mecânica dos fluidos e desafios na medida da equação de Bernoulli modificada, além da variabilidade da relação da área anatômica do orifício da válvula, dependendo da forma do orifício visto ser uma estimativa calculada por uma fórmula. Recentemente muito se tem discutido sobre a recuperação de pressão distal à vena contracta em estrutura tubular como a artéria aorta e, é claro, questões técnicas nos aspectos de medição, incluindo variabilidade temporal e hemodinâmica. Boa parte dessa discussão é muito técnica dentro dos debates de ecocardiografistas, mas saber que limitações existem é função também do clínico.
Em resumo, a baixa invasividade e disponibilidade da ecocardiografia e a capacidade de obter medições ao longo do tempo juntamente com os dados da história natural que confirmam a correlação dos gradientes com resultados clínicos suportam a uso continuado de ecocardiografia para rotina avaliação da presença de deterioração de bioprótese. Apesar dos rigorosos protocolos de aquisição, pode haver diferenças no ecocardiograma e medições invasivas de gradientes entre tipos de válvulas, tamanhos e hemodinâmica no momento da medição.
Outro aspecto que deve ser levado em consideração no acompanhamento desses pacientes é, na presença de uma elevação dos gradientes, iniciar uma investigação também da possibilidade de trombose protética. Nesse contexto, é interessante o uso da tomografia, que ganha papel preponderante.
Uma vez diante da suspeita de deterioração ou trombose, as imagens da tomografia podem esclarecer a presença de espessamentos, como o chamado HALT e HAM e também da alteração de mobilidade de folhetos protéticos. Esses achados podem ser decisórios para iniciar a anticoagulação oral e reavaliar após 2-3 meses.
Quando abordamos a valva aórtica, alguns aspectos são cruciais na tomada de decisão entre TAVI e cirurgia convencional e isso pode ser ainda mais desafiador em pacientes com anel aórtico pequeno. A compreensão de que o anel aórtico tem que acomodar uma prótese inteira constituída de anel, tecido protético, folhetos acaba levando a uma área efetiva bem menor do que o desejado em situações com limitações anatômicas e conviver com o mismatch acaba impactando negativamente a curva de sobrevida.
Aqui vale mencionar que marcas distintas de próteses ainda podem apresentar parâmetros diferentes de medidas, embora exista uma tentativa de padronização desses parâmetros que deveriam constar na bula da prótese.
Um gradiente transprotético médio acima de 20mmHg em uma prótese implantada na topografia aórtica já no pós operatório imediato é um grande indício de mismatch, mas algumas situações como hiperfluxo precisam ser excluídos, como leak para protético, estados hiperdinâmicos, etc.
Os dados de literatura mostram que a incidência de mismatch é maior em casos de abordagem cirúrgica convencional do que no TAVI, explicado em partes pela tecnologia empregada na construção das próteses transcateter e por métodos distintos de mensuração da área efetiva de fluxo protético. (Confira mais detalhes sobre este assunto em: https://d3gjbiomfzjjxw.cloudfront.net/disfuncao-de-protese-biologica-aortica-fazer-valve-in-valve/)
Estratégias cirúrgicas para melhorar hemodinâmica da prótese e os resultados clínicos incluem alargamento da raiz da aorta, próteses com stent e folhetos implantados em posição supra-anular, próteses sem stent e biopróteses sem sutura. Além desses, também merece menção o procedimento de Ross, com suas características técnicas.
O alargamento cirúrgico da raiz da aorta traz alguns riscos como maior tempo de circulação extracorpórea, sangramento da linha de sutura, e risco potencial de lesão iatrogênica da valva mitral visto termos a contiguidade do anel fibroso aórtico e mitral. No estudo STS em banco de dados norteamericano, o aumento da raiz foi realizado em apenas 2,9% de todos as abordagens cirúrgicas. Posicionamento supra-anular dos folhetos pode melhorar a hemodinâmica em comparação com o intra-anular, mas em séries cirúrgicas, isso não necessariamente se traduz em benefícios significativos a longo prazo no tocante à sobrevida ou à prevenção de eventos adversos importantes relacionados à deterioração.
REFERÊNCIA
Herrmann HC, Pibarot P, Wu C, Hahn RT, Tang GHL, Abbas AE, Playford D, Ruel M, Jilaihawi H, Sathananthan J, Wood DA, De Paulis R, Bax JJ, Rodes-Cabau J, Cameron DE, Chen T, Del Nido PJ, Dweck MR, Kaneko T, Latib A, Moat N, Modine T, Popma JJ, Raben J, Smith RL, Tchetche D, Thomas MR, Vincent F, Yoganathan A, Zuckerman B, Mack MJ, Leon MB; Heart Valve Collaboratory. Bioprosthetic Aortic Valve Hemodynamics: Definitions, Outcomes, and Evidence Gaps: JACC State-of-the-Art Review. J Am Coll Cardiol. 2022; 80(5):527-544. https://www.sciencedirect.com/science/article/abs/pii/S0735109722051592?via%3Dihub